Amerykańska Agencja Żywności i Leków – FDA (Food and Drugs Administration) dopuściła do kolejnego – ostatniego etapu homologacji (dopuszczenia do użytku) minipompę ITCA 650 dla diabetyków typu 2. Urządzenie jest produkowane przez bostońską firmę farmaceutyczną Intracia Therapeutics.
Pompy również dla diabetyków typu 2
ITCA 650 to jednoroczne minipompy, których stosowanie w połączeniu z zażywaniem metforminy może być przełomowym sposobem leczenia cukrzycy typu 2 we wczesnym jej stadium. Cukrzyca Polska pisała o wcześniejszych pracach nad tą pompą w 2014 roku.
Przeczytaj więcej jak dokładnie działa ITCA 650:
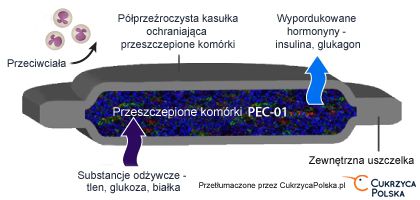
Mini-pompa składa się z umieszczanego pod skórą brzucha urządzenia (DURO) wielkości zapałki, którego zadaniem jest stałe dostarczanie eksenatydu. Eksenatyd jest lekiem inkretynowym – analogiem GLP-1.
Leki inkretynowe w obecnej formie podawane są pod postacią zastrzyków dwa razy w ciągu dnia, bądź raz w ciągu tygodnia i działają poprzez pobudzenie komórek trzustki, a co za tym idzie zwiększają wydzielanie insuliny oraz tłumią wydzielanie przez wątrobę glukagonu podnoszącego poziom cukru we krwi.
Eksenatyd został skomercjalizowany przez AstraZeneca i dostępny jest pod handlowymi nazwami Byetta i Bydureon. Pompa sprawi, ze pamiętanie o zastrzykach przestanie być koniczne, co poprawi jakość leczenia cukrzycy.
- Przeczytaj więcej na temat leków inkretynowych
Badania nad bezpieczeństwem urządzenia nadal trwają
Intracia Therapeutics czeka obecnie na ostateczną akceptację przez FDA swoich minipomp ITCA 650. na którymi pracuje od 2012 roku. Jest to już ostatni etap – tak zwana NDA (New Drug Application) , jeśli zakończy się sukcesem, oznaczać to będzie, że urządzenie odpowiada wymogom FDA i i stanie się nową terapią wykorzystywaną w leczeniu cukrzycy typu 2. Istnieje duże prawdopodobieństwo ze następnie trafi do Europy..
W ramach przygotowań do ostatniego etapu, minipopmpa ITCA 650 szastała poddana 52-tygodniowym badaniom FREEDOM-2 przeprowadzonym u 532 dorosłych z cukrzycą typu 2 leczonych metforminą.
Wyniki tych badań przedstawione podczas spotkania Amerykańskiego Stowarzyszenia Diabetyków, że ITCA 650 przyczynia się do poprawy codziennej kontroli poziomu glikemii, pozytywnych wyników HbA1c oraz zwiększa redukcję wagi, niż przy stosowaniu przez 52 tygodnie innego doustnego leku obniżającego stężenie cukru we krwi – Januvia (sitagliptin).
Minipompa nie stanowi ryzyka dla układu sercowego
Poza pozytywnymi wynikami w leczeniu cukrzycy, ITCA 650 osiągnęła również zadowalające rezultaty w trwającej 3 lata sercowo-naczyniowej próbie FREEDOM, mierzącej ryzyko wystąpienia wylewów, ataków serca oraz bóli w klatce piersiowej związanych z zastosowaniem minipompy.
Badania nad bezpieczeństwem urządzenia obejmowały ponad 4000 uczestników. Urządzenie okazało się być równie bezpieczne co placebo, co oznacza, że nie stanowiło ono zagrożenia dla stanu zdrowia układu sercowo-naczyniowego, natomiast czy faktycznie go polepszyło, nie zostało jeszcze do końca ustalone. Wiadomym jest jednak, że prawdopodobieństwo wystąpienia poważnych dysfunkcji związanych z sercem nie przekraczało granicy bezpieczeństwa.
Choć nie brzmi to szczególnie zachęcająco, to właśnie fakt czy pompa zwiększa ryzyko problemów z układem krążenia ma ogromny wpływ na dalsze losy urządzenia, z punktu widzenia Intracia Therapeutics, wyniki te były więc bardzo pozytywne.
Jeżeli urządzenie pozytywnie przejdzie ostatni etap, ma szansę na komercjalizację i będzie dostępne do końca 2017 roku w USA, a następnie w innych krajach.
Czy i kiedy będzie dostępne w Polsce – nie wiadomo.